Soll ich den Methylierungs-Enhancer verwenden?
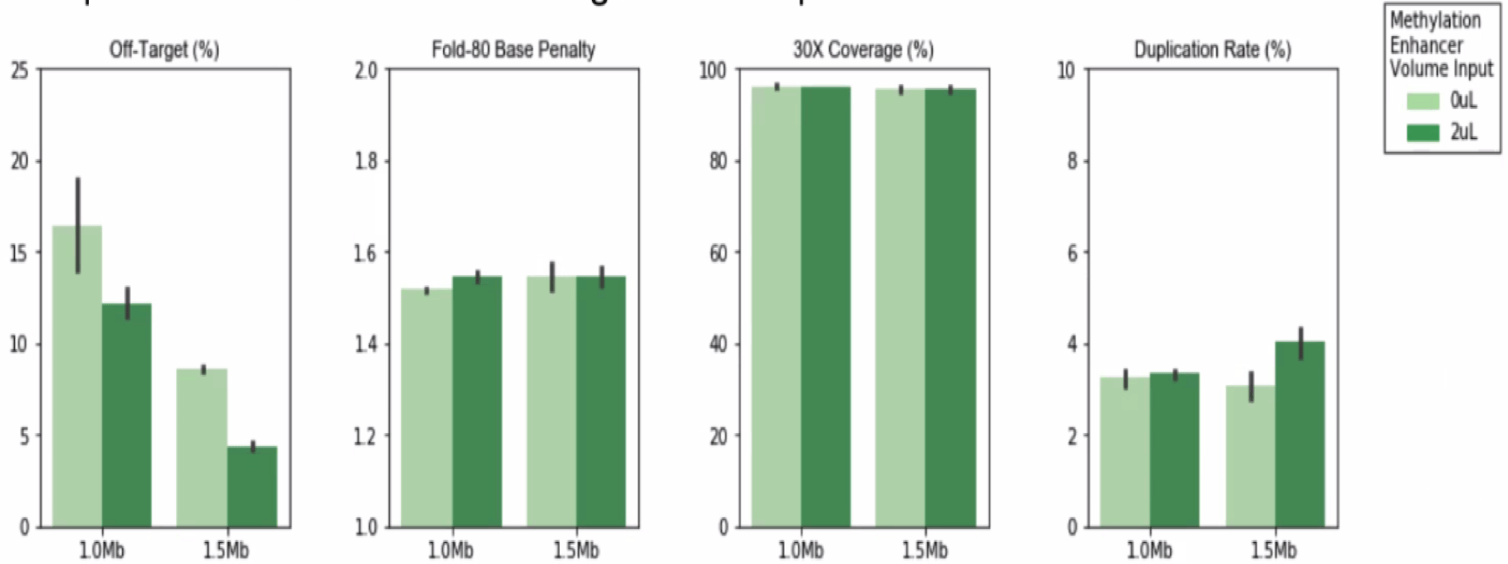
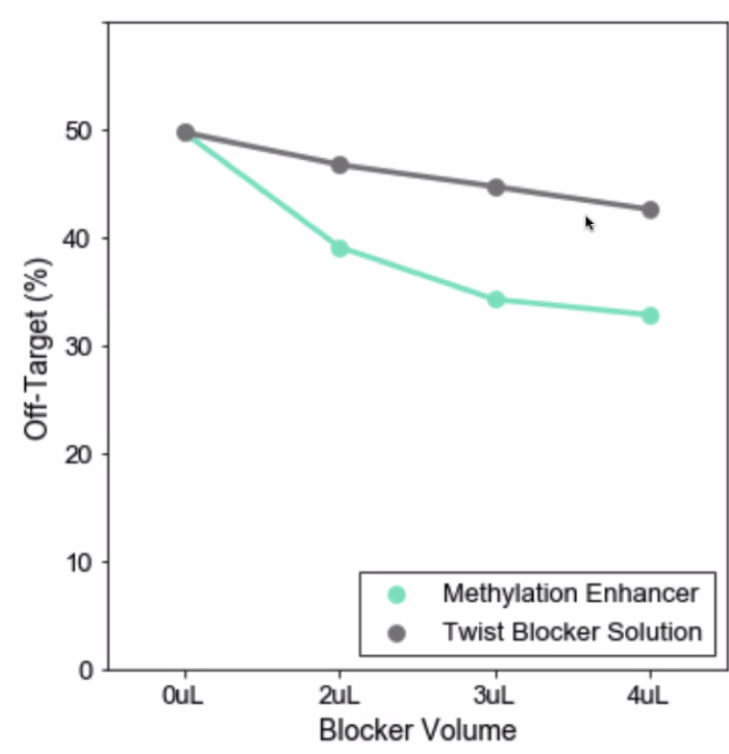
Wenn diese Reagenzien verwendet werden, hat dies auf die Hybridselektionsmetriken keinen Einfluss. Sie reduzieren Off-Target auf unterschiedliche Weise, je nach den benutzerdefinierten Zielregionen des Methylierungs-Panels und den Methylierungszuständen der hinzugefügten genomischen DNA. Bei einigen benutzerdefinierten Panels kann die Off-Target-Reduktion bis zu 50 % betragen.
War dieser Artikel hilfreich?
Ja
Nein
Sie haben noch Fragen? Kontakt
